RESUMEN
Introducción: El manejo nutricional del paciente con cáncer gástrico resulta interesante por su evolución clínica y la calidad de vida. La desnutrición asociada a la enfermedad representa un desafío relevante en la práctica asistencial. Objetivo: Describir el abordaje nutricional en pacientes con cáncer gástrico mediante una revisión bibliográfica actualizada. Método: Se desarrolló una investigación con enfoque mixto, de predominio cualitativo, carácter descriptivo y aplicado, sustentada en una revisión sistemática de literatura reciente y de alto impacto en español e inglés. Resultado: La evidencia analizada identifica la nutrición enteral como estrategia preferente, considerando el estado nutricional, el estadio de la enfermedad y los tratamientos recibidos, como quimioterapia, radioterapia o cuidados paliativos. Asimismo, se observó que una intervención nutricional oportuna mejora la tolerancia terapéutica y la respuesta clínica. Conclusiones: Un manejo nutricional integral y personalizado es fundamental para optimizar resultados terapéuticos y favorecer la recuperación del paciente con cáncer gástrico.
Descriptores: cáncer gástrico; manejo nutricional; nutrición; quimioterapia; radioterapia. (Fuente: DeCS).
ABSTRACT
Introduction: Nutritional management of patients with gastric cancer is interesting due to their clinical progression and quality of life. Malnutrition associated with the disease represents a significant challenge in healthcare practice. Objective: To describe the nutritional approach in patients with gastric cancer through an updated literature review. Method: A mixed-method research study was conducted, predominantly qualitative, descriptive, and applied, based on a systematic review of recent, high-impact literature in Spanish and English. Results: The evidence analyzed identifies enteral nutrition as the preferred strategy, considering nutritional status, disease stage, and treatments received, such as chemotherapy, radiotherapy, or palliative care. It was also observed that timely nutritional intervention improves therapeutic tolerance and clinical response. Conclusions: Comprehensive and personalized nutritional management is essential to optimize therapeutic outcomes and promote recovery in patients with gastric cancer.
Descriptors: gastric cancer; nutritional management; nutrition; chemotherapy; radiotherapy. (Source: DeCS).
INTRODUCCIÓN
El cáncer gástrico continúa siendo una de las neoplasias más frecuentes y letales a nivel mundial; constituye la cuarta causa principal de muerte en ambos sexos y cada año se diagnostican más de un millón de casos ¹. En Ecuador representa la principal causa de mortalidad oncológica, con el 13,3% de los decesos por esta causa ². Su carácter frecuentemente asintomático favorece el diagnóstico tardío, condición que se asocia a elevada prevalencia de desnutrición, la cual empeora el pronóstico clínico ³.
La desnutrición es un problema relevante durante la progresión tumoral y en el curso de los tratamientos oncológicos ⁴, ya que deteriora la recuperación, disminuye la capacidad funcional y afecta la calidad de vida. Por ello, la evaluación e intervención nutricional tempranas son esenciales en el manejo integral del paciente ⁵. Un adecuado abordaje nutricional en las fases clínica, perioperatoria, postoperatoria y paliativa mejora el estado inmunológico, reduce complicaciones y estancia hospitalaria, aunque la evidencia sobre su impacto en morbilidad y mortalidad aún es limitada ³ ⁶.
El Fondo Mundial para la Investigación del Cáncer/Instituto Americano para la Investigación del Cáncer señala que una alimentación inadecuada, caracterizada por consumo de carnes procesadas y alimentos conservados en sal, incrementa el riesgo de cáncer gástrico ⁷. En estos pacientes, la desnutrición deriva tanto de alteraciones metabólicas propias de la enfermedad como de efectos adversos terapéuticos que disminuyen la ingesta y absorción. El soporte nutricional debe sustentarse en evaluación y asesoramiento especializados, incluyendo dietas artificiales orientadas a prevenir la pérdida ponderal y optimizar el estado clínico.
El abordaje nutricional debe integrarse en todas las etapas terapéuticas, desde la cirugía hasta el cuidado paliativo, mediante nutrición oral, nutrición enteral (NE) o nutrición parenteral total (NPT). La nutrición oral se ajusta a la tolerancia del paciente; la NE, administrada por sonda, se indica cuando la vía oral es insuficiente ⁸; y la NPT, por vía intravenosa, se reserva para casos con función gastrointestinal comprometida ⁹.
La cirugía constituye un pilar terapéutico. La desnutrición preoperatoria compromete la inmunidad y la cicatrización, interfiriendo con la quimioterapia adyuvante y la recuperación. La NE preoperatoria favorece la digestión, absorción y motilidad intestinal, contribuyendo a mejores resultados clínicos ¹⁰. Gao et al. ¹¹ demostraron que la alimentación postoperatoria temprana tras gastrectomía radical laparoscópica mejora la función gastrointestinal y reduce complicaciones. Asimismo, la NE domiciliaria ha mostrado ser segura y eficaz para mantener el peso y mejorar el pronóstico en pacientes desnutridos ¹².
La NPT está indicada cuando se requiere reposo intestinal prolongado, tanto en hospitalización como en cuidados paliativos, especialmente en casos de deterioro progresivo o caquexia avanzada ¹³. En el cáncer avanzado, el abordaje multidisciplinario es fundamental. Las guías de la ESPEN recomiendan evaluación nutricional periódica mediante herramientas como la SGA o la NRS 2002, que permiten identificar riesgo y orientar la intervención ¹⁴.
Los cuidados de enfermería en la rehabilitación posquirúrgica favorecen la recuperación gastrointestinal y psicológica, reducen complicaciones y mejoran la calidad de vida ¹⁵. En fase terminal, la intervención nutricional debe individualizarse y extenderse a familiares y cuidadores, priorizando el confort y la calidad de vida ¹⁶. En este contexto, el presente artículo tiene como objetivo describir la nutrición en pacientes con cáncer gástrico mediante una revisión bibliográfica, analizando las principales alternativas terapéuticas disponibles.
MÉTODO
Según el enfoque de investigación, el presente artículo corresponde a una investigación mixta, con predominio cualitativa, que se caracteriza por describir la importancia de la nutrición en pacientes con cáncer gástrico, destacando las investigaciones más evidentes. Según su alcance se considera descriptiva, en esta investigación se quiere dar a conocer que el abordaje nutricional (valoración e intervención), en los pacientes con cáncer gástrico repercute en la tolerancia a los tratamientos, pronóstico y calidad de vida.
Según la finalidad, la presente investigación se considera aplicada, porque describe la nutrición en pacientes con cáncer gástrico en base al análisis de la información, la misma que implica relevancia al momento de planificar el tratamiento. Se efectúa una revisión bibliográfica, misma que emplea el método analítico-sintético para el procesamiento de la información necesaria para el estudio, identificar rasgos, buscar conexiones entre ideas y elaborar valoraciones y conclusiones parciales, además de establecer las conexiones internas, la secuencia lógica y los rasgos clave de los fenómenos relacionados al estudio que se plantea.
Para seleccionar la información necesaria para el desarrollo del trabajo se emplearon bases de datos y revistas indexadas, tales como PubMed, SciELO, LILACS entre otras. Los idiomas seleccionados para los artículos a escoger son el español e inglés. Se utilizan palabras clave como: nutrición, cáncer gástrico, hábitos alimenticios.
Para garantizar la rigurosidad y pertinencia del análisis bibliográfico realizado, se establecieron criterios específicos de inclusión y exclusión que orientaron la selección de las fuentes documentales.
Criterios de inclusión: Se incluyeron artículos publicados en revistas indexadas, así como libros, tesis de maestría y de especialidad, y ponencias presentadas en congresos científicos internacionales. La búsqueda se realizó en bases de datos reconocidas como PubMed, SciELO y LILACS. Se consideraron investigaciones relacionadas con nutrición en pacientes con cáncer gástrico mayores de 18 años. Con el propósito de garantizar actualidad y pertinencia científica, al menos el 50 % de la bibliografía seleccionada correspondió a artículos publicados en los últimos cinco años.
Criterios de exclusión: Se excluyeron publicaciones provenientes de periódicos y artículos difundidos en revistas no indexadas. Asimismo, no se consideraron tesis de pregrado. En relación con la población de estudio, se excluyeron investigaciones que incluyeran pacientes oncológicos menores de 18 años y pacientes en estado de gestación.
RESULTADOS
En esta sección se sintetizan y analizan de manera integrada los principales hallazgos identificados en los estudios seleccionados, evidenciando la estrecha relación entre estado nutricional, evolución clínica y resultados terapéuticos en pacientes con cáncer gástrico. Arista ¹⁷ señala que el cáncer gástrico, quinta neoplasia en frecuencia en América Latina, suele diagnosticarse en fases avanzadas, lo que compromete la absorción de nutrientes y favorece la desnutrición, con impacto negativo en la respuesta inmunológica. Este diagnóstico tardío no solo limita las posibilidades de tratamiento curativo, sino que agrava el deterioro metabólico progresivo, condicionando mayor vulnerabilidad a infecciones y complicaciones postoperatorias. El estudio demuestra que la nutrición enteral temprana presenta mayores beneficios clínicos que la nutrición parenteral, particularmente en términos de mantenimiento de la integridad intestinal y menor incidencia de complicaciones infecciosas. Tales resultados refuerzan la necesidad de instaurar intervenciones nutricionales oportunas como parte del protocolo inicial de atención.
En este contexto, la nutrición oral se refiere a la ingesta por vía fisiológica con o sin suplementos; la nutrición enteral implica la administración de nutrientes a través de sonda al tracto gastrointestinal funcional; y la nutrición parenteral consiste en el aporte intravenoso de nutrientes cuando el tracto digestivo no puede utilizarse. Esta diferenciación conceptual resulta fundamental para la adecuada toma de decisiones clínicas, ya que cada modalidad responde a indicaciones específicas y perfiles de riesgo diferenciados. La selección del tipo de soporte debe basarse en la funcionalidad gastrointestinal, el estado hemodinámico y la fase del tratamiento oncológico. Desde una perspectiva fisiológica, la nutrición enteral preserva la barrera mucosa y estimula la motilidad intestinal, mientras que la parenteral, aunque eficaz en situaciones de imposibilidad digestiva, se asocia a mayor riesgo de complicaciones metabólicas y sépticas. Por ello, la jerarquización de las modalidades no es arbitraria, sino sustentada en criterios clínicos y evidencia acumulada.
El índice pronóstico nutricional se relaciona estrechamente con la supervivencia posterior a gastrectomía. Miranda ¹⁸ evidenció que valores bajos se asocian con menor supervivencia global y libre de recaída, así como con mayor incidencia de complicaciones postoperatorias, respaldando su utilidad como herramienta predictiva. Este indicador integra parámetros bioquímicos e inmunológicos que permiten estimar la reserva funcional del paciente antes de la intervención quirúrgica. Su aplicación sistemática facilita la estratificación de riesgo y la planificación de estrategias de soporte individualizadas. Además, su valor predictivo refuerza la premisa de que el estado nutricional no constituye una variable secundaria, sino un determinante pronóstico de relevancia clínica. En consecuencia, la evaluación nutricional debe formar parte de la valoración preoperatoria estándar.
Kubota et al. ¹⁹ destacan que sociedades científicas recomiendan la nutrición oral/enteral temprana, estrategia asociada a seguridad, viabilidad y reducción de estancia hospitalaria ²⁰. Esta recomendación se enmarca en protocolos de recuperación mejorada, donde la alimentación precoz contribuye a restablecer la función intestinal y disminuir complicaciones. Garla et al. ²¹ enfatizan la detección precoz de trastornos nutricionales para prevenir complicaciones y mejorar supervivencia, subrayando la importancia del tamizaje sistemático desde el diagnóstico. En pacientes caquécticos, el soporte nutricional pre y postoperatorio es indispensable; aunque la nutrición parenteral ofrece rápida provisión, incrementa el riesgo séptico ²², lo que obliga a una evaluación rigurosa de riesgo-beneficio antes de su indicación. Estos hallazgos evidencian la necesidad de un abordaje equilibrado, sustentado en criterios clínicos objetivos y monitorización constante.
Aoyama et al. ²³ subrayan la necesidad de evaluar estado nutricional e inflamación durante el tratamiento multidisciplinar, considerando que la respuesta inflamatoria sistémica influye en la evolución clínica y en la tolerancia terapéutica. En cuidados paliativos, el soporte nutricional debe indicarse cuando los beneficios superen riesgos y exista consentimiento informado ²⁴; incluso se documentan decisiones de nutrición parenteral prolongada en contextos de enfermedad avanzada ²⁵. Estas situaciones plantean dilemas ético-clínicos relacionados con la proporcionalidad terapéutica y los objetivos de cuidado centrados en la calidad de vida. La toma de decisiones debe fundamentarse en la valoración individual, el pronóstico y las preferencias del paciente, evitando intervenciones fútiles o desproporcionadas. Así, la nutrición en etapas avanzadas exige no solo criterios clínicos, sino también sensibilidad ética.
Tras gastrectomía total, se describen dietas fraccionadas, hipolipídicas y suplementación con fórmulas poliméricas ²⁶, orientadas a facilitar la digestión y reducir síntomas como el síndrome de dumping. Malik et al. ²⁷ evidenciaron que la vitamina B12 oral en dosis farmacológicas es comparable a la vía parenteral y señalan el papel potencial del GLP-1 en el síndrome de dumping (GLP-1, Glucagon-Like Peptide-1; péptido similar al glucagón tipo 1), lo que abre perspectivas terapéuticas relevantes en el manejo metabólico postquirúrgico. En pacientes sometidos a quimioterapia y radioterapia, el soporte nutricional mejora tolerancia terapéutica, calidad de vida y limita la pérdida ponderal ²⁸ ²⁹, confirmando su impacto positivo en la continuidad del tratamiento oncológico. Finalmente, los pacientes postgastrectomía presentan alto riesgo de desnutrición, por lo que se requieren intervenciones orientadas a mitigar síntomas gastrointestinales y optimizar el estado nutricional ²⁰ (Figura 1). En conjunto, estos resultados consolidan la evidencia de que la intervención nutricional debe ser planificada, continua y adaptada a cada fase del proceso terapéutico, con el objetivo de mejorar resultados clínicos y preservar la calidad de vida.
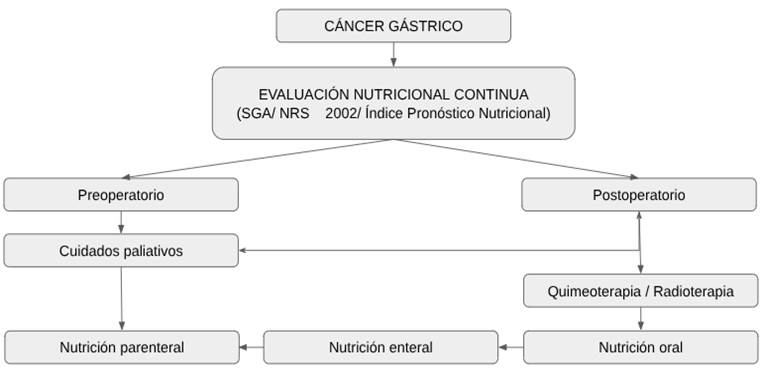
Figura 1. Soporte nutricional para el cáncer gástrico.
Elaboración: Los autores.
DISCUSIÓN
El análisis comparativo de los estudios revisados permitió identificar convergencias sustanciales y algunas discrepancias relevantes en torno al manejo nutricional del cáncer gástrico. De manera consistente, la literatura coincide en reconocer esta neoplasia como una de las principales causas de mortalidad a nivel mundial, lo que ha motivado un creciente interés científico en el perfeccionamiento de estrategias terapéuticas integrales, entre ellas el abordaje nutricional como componente esencial del tratamiento ²⁴. Sin embargo, esta prioridad contrasta con la elevada carga de complicaciones clínicas y metabólicas asociadas a la enfermedad, las cuales continúan representando un desafío para la práctica asistencial ²⁰. Esta aparente contradicción pone de manifiesto que el reconocimiento teórico de la relevancia del soporte nutricional no siempre se traduce en su implementación sistemática. En términos críticos, ello sugiere la persistencia de brechas entre la evidencia científica disponible y la práctica clínica real, condicionadas por factores estructurales, organizativos y formativos. Por tanto, la discusión debe trascender la mera descripción de hallazgos y orientarse hacia el análisis de cómo operacionalizar las recomendaciones en contextos asistenciales concretos.
Un eje transversal en los estudios examinados es la consideración de la nutrición como pilar complementario e inseparable del tratamiento oncológico ²⁴. Diversos autores subrayan que el soporte nutricional no debe entenderse como una medida accesoria, sino como parte estructural del plan terapéutico ²⁴. En esta línea, se enfatiza la necesidad de que el personal médico integre la prescripción nutricional desde el inicio del tratamiento, articulando de manera sinérgica la terapia antineoplásica con el soporte metabólico ²⁰ ²³. Esta perspectiva refuerza el enfoque interdisciplinario como estándar de calidad asistencial. Desde una visión reflexiva, la integración temprana del soporte nutricional no solo optimiza resultados clínicos, sino que también contribuye a reducir complicaciones prevenibles y a mejorar la adherencia terapéutica. Asimismo, posiciona a la nutrición clínica como indicador de calidad y seguridad del paciente, lo cual debería impulsar la institucionalización de protocolos de evaluación nutricional obligatoria en los servicios oncológicos.
La vulnerabilidad nutricional de estos pacientes constituye otro punto de consenso. Las manifestaciones clínicas -náuseas, vómitos, obstrucción y dolor abdominal-, junto con las alteraciones metabólicas inducidas por la enfermedad, incrementan significativamente el riesgo de desnutrición ²⁶. La evidencia muestra que el estado nutricional deficiente se asocia con menor capacidad de recuperación postquirúrgica, deterioro de la respuesta inmunológica, baja tolerancia a la terapia antineoplásica y mayor susceptibilidad a infecciones ²⁸ ¹³. En consecuencia, se recomienda instaurar precozmente intervenciones nutricionales tras el diagnóstico, que pueden abarcar desde modificaciones dietéticas orales hasta la implementación de soporte enteral o parenteral ²⁴. Desde una perspectiva crítica, estos hallazgos permiten comprender que la desnutrición no es únicamente un efecto colateral de la enfermedad, sino un determinante pronóstico que influye directamente en la evolución clínica. Por ello, el cribado nutricional sistemático debería considerarse una práctica estándar y no una medida opcional, garantizando seguimiento continuo y ajustes dinámicos según la respuesta del paciente.
En cuanto a la modalidad de soporte, predomina la recomendación de la nutrición enteral como primera elección siempre que el tracto gastrointestinal sea funcional ²⁴. Su carácter fisiológico y su impacto favorable en la recuperación de la motilidad intestinal postoperatoria sustentan esta preferencia ²³ ²⁷. No obstante, algunos estudios advierten que la selección del tipo de soporte debe individualizarse según la técnica quirúrgica practicada ²⁷ ²⁶, lo que introduce un matiz clínico relevante y evita generalizaciones excesivas. Este enfoque individualizado resulta coherente con los principios de la medicina personalizada, en la que las decisiones terapéuticas se adaptan a las condiciones anatómicas y funcionales del paciente. Asimismo, refuerza la necesidad de evaluación continua y de una toma de decisiones flexible basada en criterios clínicos.
Tras gastrectomía subtotal, la administración mediante sonda nasoyeyunal suele considerarse más segura que la nasogástrica por el menor riesgo de broncoaspiración y reflujo. En gastrectomía total, la yeyunostomía puede constituir una alternativa viable cuando la vía nasoyeyunal no es factible. Estas decisiones reflejan la necesidad de preservar la funcionalidad intestinal y optimizar la absorción en el período postoperatorio. Además, evidencian que el soporte nutricional no puede estandarizarse de forma rígida, sino que requiere valoración quirúrgica y metabólica integral. La adecuada elección de la vía de administración influye no solo en la tolerancia, sino también en la prevención de complicaciones asociadas al procedimiento.
La intervención nutricional también se asocia con mejoras significativas en la calidad de vida, particularmente en pacientes sometidos a gastrectomía total o a quimio-radioterapia ²¹. Incluso en cuidados paliativos, el soporte nutricional puede contribuir al confort y bienestar global del paciente ²¹. Estos resultados amplían la visión del soporte nutricional más allá de la supervivencia, incorporando dimensiones de funcionalidad, autonomía y bienestar subjetivo. No obstante, emerge una discrepancia relevante respecto al manejo en etapa terminal. Aunque se reconoce la centralidad de la nutrición en el control de la enfermedad, algunos estudios recomiendan de manera predominante la nutrición parenteral en cuidados paliativos avanzados, especialmente ante dolor intenso o imposibilidad de vía enteral. Esta recomendación abre un debate ético-clínico sobre proporcionalidad terapéutica, futilidad médica y objetivos centrados en la dignidad del paciente, lo que exige decisiones individualizadas basadas en el balance riesgo-beneficio y en los valores del paciente.
Finalmente, se observa una marcada concentración geográfica de la evidencia en Asia, particularmente en China, lo que limita la extrapolación a contextos latinoamericanos. Esta brecha evidencia la necesidad de investigaciones regionales que permitan contextualizar las recomendaciones y fortalecer el desarrollo de estrategias dietéticas culturalmente pertinentes orientadas a mejorar la calidad de vida de los pacientes con cáncer gástrico. La variabilidad epidemiológica, sociocultural y de recursos sanitarios puede influir significativamente en la aplicabilidad de las intervenciones descritas. Por ello, resulta imprescindible promover estudios multicéntricos en América Latina que generen evidencia contextualizada y favorezcan la adaptación de protocolos nutricionales a realidades locales. Solo mediante este enfoque será posible consolidar una práctica clínica basada en evidencia robusta, pertinente y socialmente sostenible.
CONCLUSIONES
El análisis crítico de la evidencia disponible confirma que el soporte nutricional constituye un componente esencial en el abordaje integral del cáncer gástrico, con impacto directo en la evolución clínica, la tolerancia terapéutica y la calidad de vida.
La nutrición enteral se posiciona como la primera opción terapéutica en pacientes con cáncer gástrico siempre que el tracto gastrointestinal sea funcional, debido a su carácter más fisiológico y a su perfil de seguridad en comparación con la nutrición parenteral.
Puede aplicarse en distintos estadios de la enfermedad, incluyendo fases moderadas y cuidados paliativos, siempre bajo una valoración clínica individualizada que considere el estado general y los objetivos terapéuticos.
El soporte nutricional mejora resultados clínicos al favorecer la recuperación postoperatoria, fortalecer la respuesta inmunológica y aumentar la tolerancia a los tratamientos oncológicos. La selección del tipo de nutrición debe individualizarse, considerando factores como la realización de gastrectomía total o parcial, el esquema terapéutico recibido y las condiciones metabólicas del paciente.
El abordaje debe ser integral e interdisciplinario, incorporando educación nutricional, acompañamiento psicosocial y criterios éticos en la toma de decisiones, con el fin de optimizar beneficios clínicos y preservar la calidad de vida.
CONFLICTO DE INTERÉS
Los autores declaran que no tienen conflicto de interés en la publicación de este artículo.
FINANCIAMIENTO
Autofinanciado.
AGRADECIMIENTO
A todos los agentes sociales involucrados en el desarrollo de la investigación.
REFERENCIAS
1. Organización Mundial de la Salud. Cáncer. 2022. https://n9.cl/blzd
2. Ferlay J, Ervik M, Lam F, Colombet M, Mery L, Piñeros M, et al. Global Cancer Observatory: Cancer Today. Lyon, France: International Agency for Research on Cancer. 2020. https://gco.iarc.fr/today
3. Rosania R, Chiapponi C, Malfertheiner P, Venerito M. Nutrition in Patients with Gastric Cancer: An Update. Gastrointest Tumors. 2016;2(4):178-187. https://doi.org/10.1159/000445188
4. Kubota T, Shoda K, Konishi H, Okamoto K, Otsuji E. Nutrition update in gastric cancer surgery. Ann Gastroenterol Surg. 2020;4(4):360-368. https://doi.org/10.1002/ags3.12351
5. Gharagozlian S, Mala T, Brekke H, Kolbjørnsen L, Ullerud Ä, Johnson E. Nutritional status, sarcopenia, gastrointestinal symptoms and quality of life after gastrectomy for cancer - A cross-sectional pilot study. Clin Nutr ESPEN. 2020;37:195-201. https://doi.org/10.1016/j.clnesp.2020.03.001
6. Hsu O, Chuah S, Lin J, Huang S, Lo J, Rau K, et al. Taiwan nutritional consensus on the nutrition management for gastric cancer patients receiving gastrectomy. J Formos Med Assoc. 2021;120(1):25-33. https://doi.org//10.1016/j.jfma.2019.11.014
7. Clinton S, Giovannucci E, Hursting S. The World Cancer Research Fund/American Institute for Cancer Research Third Expert Report on Diet, Nutrition, Physical Activity, and Cancer: Impact and Future Directions. J Nutr. 2020;150(4):663-671. https://doi.org/10.1093/jn/nxz268
8. Weimann A, Braga M, Harsanyi L, Laviano A, Ljungqvist O, Soeters P. ESPEN Guidelines on Enteral Nutrition: Surgery including organ transplantation. Clin Nutr. 2006;25(2):224-244. https://doi.org/10.1016/j.clnu.2006.01.015
9. Bozzetti F, Arends J, Lundholm K, Zurcher G, Muscaritori M, ESPEN. ESPEN Guidelines on Parenteral Nutrition: non-surgical oncology. Clin Nutr. 2009;28(4):445-454. https://doi.org/:10.1016/j.clnu.2009.04.011
10. Li J, Li S, Xi H, Liu P, Liang W, Gao Y, et al. Effect of preoperative nutrition therapy type and duration on short-time outcomes in gastric cancer patient with gastric outlet obstruction. Chin J Cancer. 2021;33(2):232-242. https://doi.org/10.21147/j.issn.1000-9604.2021.02.10
11. Gao L, Zhao Z, Zhang L, Shao G. Effect of early oral feeding on gastrointestinal function recovery in postoperative gastric cancer patients: a prospective study. J BUON. 2019;24(1):194-200. https://n9.cl/j22gff
12. Gavazzi C, Colatruglio S, Valoriani F, Mazzaferro V, Sabbatini A, Biffi R, et al. Impact of home enteral nutrition in malnourished patients with upper gastrointestinal cancer: A multicentre randomised clinical trial. Eur J Cancer. 2016;64:107-112. https://n9.cl/450sl
13. Bozzetti F. The role of parenteral nutrition in patients with malignant bowel obstruction. Support Care Cancer. 2019;27(12):4393-4399. https://doi.org/10.1007/s00520-019-04948-1
14. Kazmierczak K, Skonieczna K, Folwarski M, Ruszkowski J, Swierblewski M, Makarewicz W. Influence of malnutrition stage according to GLIM 2019 criteria and SGA on the quality of life of patients with advanced cancer. Nutr Hosp. 2020;27(6):1179-1185. https://doi.org/10.3389/fnut.2022.1030619
15. Wang Y, Zhou Q. The effect of accelerated rehabilitation nursing on postoperative recovery, nutritional status, and psychological status in patients with gastric cancer. Am J Transl Res. 2021;13(4):3666-3673. https://n9.cl/gtl0m
16. Prevost V, Grach M. Nutritional support and quality of life in cancer patients undergoing palliative care. Eur J Cancer Care. 2012;21(5):581-590. https://doi.org/10.1111/j.1365-2354.2012.01363.x
17. Arista Y. Revisión crítica: Terapia nutricional en pacientes con cáncer gástrico. 2020. https://n9.cl/qqfmk
18. Miranda D. Revisión crítica: valor predictivo del índice pronóstico nutricional en pacientes con cáncer gástrico. 2021. https://acortar.link/4UGmmJ
19. Kubota T, Shoda K, Konishi H, Okamoto K, Otsuji E. Nutrition update in gastric cancer surgery. Ann Gastroenterol Surg. 2020;4(4):360-368. https://doi,org/10.1002/ags3.12351
20. Arrufat J. Beneficios de la nutrición oral temprana en el paciente gastrectomizado por cáncer. Una revisión integradora. 2022. https://repositori.uji.es/xmlui/handle/10234/200951
21. Garla P, Linetzky D, Tesser A. Nutritional Therapy in Gastrointestinal Cancers. Gastroenterol Clin North Am. 2018;47(1):231-242. https://n9.cl/je24hr
22. Stojcev Z, Matysiak K, Duszewski M, Banasiewicz T. The role of dietary nutrition in stomach cancer. Contemp Oncol (Pozn). 2013;17(4). https://doi.org/10.5114/wo.2013.37213
23. Aoyama T, Hara K, Kazama K, Maezawa Y. Clinical Impact of Nutrition and Inflammation Assessment Tools in Gastric Cancer Treatment. Anticancer Res. 2022;42(11). https://doi.org/10.21873/anticanres.16023
24. Camblor M, Ocón M, Luengo M, Virizuela J, Sendrós M, Cervera M, et al. Soporte nutricional y nutrición parenteral en el paciente oncológico: informe de consenso de un grupo de expertos. Nutr Hosp. 2018;15(1). https://doi.org/10.1016/j.endinu.2017.10.012
25. Maza C, Gonzalez L, Corado M. Abordaje nutricional de un paciente en cuidados paliativos. Análisis de un caso clínico. Rev Nutr Clin Metab. 2020;4(2). https://doi.org/10.35454/rncm.v4n2.233
26. Poma D, Alcántara M. Manejo nutricional en un paciente con gastrectomía total. Rev Esp Nutr (ReNut). 2012;6(2). https://acortar.link/LDc6nK
27. Malik S, Semrad C. Nutritional Implications in Preparing Patients for Total Gastrectomy. Curr Surg Rep. 2020;8(27). https://doi.org/10.1007/s40137-020-00273-3
28. Qiu M, Zhou Y, Jin Y, Wang Z, Wei X, Han H, et al. Nutrition support can bring survival benefit to high nutrition risk gastric cancer patients who received chemotherapy. Support Care Cancer. 2015;23. https://doi.org/10.1007/s00520-014-2523-6
29. Isenring E, Capra S, Bauer J. Nutrition intervention is beneficial in oncology outpatients receiving radiotherapy to the gastrointestinal or head and neck area. Br J Cancer. 2004;91. https://doi.org/10.1038/sj.bjc.6601962
©2026 por los autores. Este artículo es de acceso abierto y distribuido según los términos y condiciones de la licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional (CC BY-NC-SA 4.0) (https://creativecommons.org/licenses/by-nc-sa/4.0/)